تجهیزات مورد استفاده در تولید دارو نیاز به رعایت صلاحیت مداوم برای نظارت بر عملکرد آن دارند
.
چرا به احراز صلاحیت نیاز داریم؟
چهارچوب کاری لازم جهت اخذ صلاحیت تجهیزات دارویی قبل از راه اندازی چیست؟
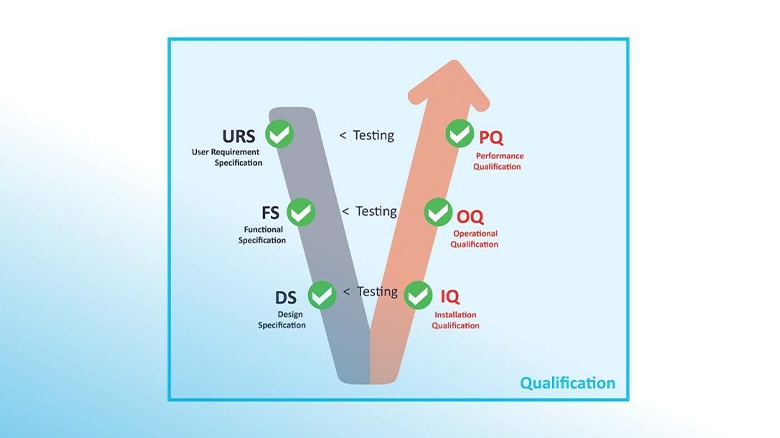
مشخصات مورد نیاز کاربر (URS)
مشخصات مورد نیاز کاربر شامل مشخصات طراحی و مشخصات عملکردی است. مشخصات طراحی، اطلاعات صریح در مورد الزامات طراحی برای تجهیزات را ارائه می دهد؛ به عنوان مثال: ابعاد، مواد ساخت و ساز، چیدمان و غیره. مشخصات عملکردی، نشان دهنده نحوه عملکرد هر یک از ویژگی های تجهیزات یا سیستم است
.
صلاحیت طراحی (DQ)
مشخصات مورد نیاز کاربر
(USR)، که شامل مشخصات طراحی و عملکرد تجهیزات است و با جزئیات واقعی تجهیزات ارائه شده توسط تامین کننده (طراحی و عملکرد) تأیید شده است. این تعریف صلاحیت طراحی است و یک فعالیت مستندسازی بوده و توصیه می شود قبل از اجرایی شدن پروسه، تکمیل شود
.
تست پذیرش کارخانه (FAT)
FAT شامل موارد زیر است
:
آزمون پذیرش کارخانه باید در موارد زیر انجام شود
:
تست پذیرش سایت (SAT)
SAT شامل این موارد است
:
صلاحیت نصب (IQ)
تست صلاحیت نصب شامل بررسی موارد زیر است
:
صلاحیت نصب باید در موارد زیر دوباره بررسی شود
:
- جابجایی تجهیزات از یک مکان به مکان دیگر (به استثنای نوع پرتابل).
- در صورت تغییر عمده و یا رسیدگی به صلاحیت جزء جدید اضافه شده.
- IQمعمولاً بر اساس یک پروتکل از پیش تأیید شده اجرا می شود و همه نتایج باید جمع آوری و به صورت مکتوب خلاصه شوند.
صلاحیت اجرایی (OQ)
صلاحیت اجرایی باید در موارد زیر دوباره بررسی شود
:
- جابجایی تجهیزات از یک مکان به مکان دیگر (به استثنای نوع پرتابل).
- در صورت تغییر عمده یا برای رسیدگی به صلاحیت جزء جدید اضافه شده RQ شروع می شود . (RQ: Re-Qualification).
OQ
بر اساس یک پروتکل از پیش تأیید شده اجرا می شود و همه نتایج باید جمع آوری شوند
.
صلاحیت عملکرد (PQ)
PQ رویهها، پرسنل، سیستمها و مواد را یکپارچه میکند تا تأیید کند که ابزار، محیط، تجهیزات یا سیستم پشتیبانی، درجه دارویی محصول تولیدی را تضمین میکند
.
فلسفه تست، در طول طراحی پروتکل ها، بر اساس اصول و توضیحاتی که در اینجا برشمرده شده است، کنترل می شود
.
پیش نیازهای اجرای PQ عبارتند از
:
معیارهای پذیرش باید به وضوح در سند PQ
نشان داده شود
.
PQ مرحله نهایی صلاحیت است که نشان می دهد تجهیزات یا سیستم چگونه تحت شرایط تولید واقعی یا عملیات شبیه سازی شده عمل می کند. این سری از آزمایش ها برای نشان دادن توانایی تجهیزات یا سیستم در کارکرد و تولید محصول با کیفیت مشخص در بدترین حالت ممکن است. این مرحله تنها زمانی قابل انجام است که پارامترهای عملیاتی تعریف و تایید شده باشند
.
احراز صلاحیت عملکرد باید در موارد زیر دوباره بررسی شود
:
- تعویض ابزار یا قطعه موجود در تجهیزات با ابزار جدید که می تواند تأثیر مستقیمی بر عملکرد تجهیزات داشته باشد.
- هر گونه تغییر عمده در تجهیزات یا سیستم موجود که می تواند بر عملکرد تجهیزات تأثیر بگذارد.
- اگر سیستم در حین صلاحیت عملکرد (PQ)، نادرست عمل کند.
PQ در یک پروتکل از پیش تأیید شده اجرا می شود
.
احراز صلاحیت مجدد (RQ)
صلاحیت مجدد فعالیتی است که شامل همه یا بخش هایی از فعالیتهای صلاحیت، مانند
IQ، OQ و PQ است
.
صلاحیت مجدد به یک یا چند دلیل از موارد زیر انجام می شود
:
علاوه بر تست عناصر متاثر از تغییرات یا پارامترهای صلاحیتی ناقص، همه اجزای کلیدی تجهیزات برای عملکرد در طی صلاحیت مجدد تأیید می شوند
.
منبع:
https://pharmapathway.com